Myślę, że większość z nas w swojej praktyce zawodowej spotkała się z symbolem czarnego odwróconego trójkąta w ulotce lub ChPL razem z napisem: „Ten produkt leczniczy podlega dodatkowemu monitorowaniu”. (Patrz: “Czym różni się ulotka do leku od Charkterystyki Produktu Leczniczego (ChPL)?”.) Symbol ten obowiązuje w UE i oznacza leki nowe, najczęściej biologiczne, które mają mało badań dotyczących długotrwałego stosowania lub mają badania kliniczne z udziałem małych grup pacjentów.
Przykładem leku podlegającego dodatkowemu monitorowaniu jest Izotek.

EMA (podobnie jak krajowe agencje) dopuszcza dany lek do obrotu, jeżeli uzna, że korzyść z jego stosowania przewyższa ewentualne ryzyko. Następnie przez okres kilku lat zbiera dane od europejskich organów ds. rejestracji dotyczące działań niepożądanych, które wystąpiły u pacjentów stosujących ten lek. Sama procedura monitorowania jest identyczna w całej UE, dzięki czemu poszczególne kraje mogą łatwo wymieniać się informacjami.[1]
Leki podlegające dodatkowemu monitorowaniu
Symbol czarnego trójkąta dotyczy leków biologicznych, takich jak szczepionki (których skład zmienia się często, w zależności od zaleceń WHO), np. Vaxigrip Tetra.

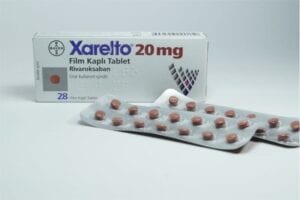
Umieszcza się go także w ChPL i ulotce leków dopuszczonych warunkowo (gdy podmiot odpowiedzialny musi przeprowadzić dodatkowe badania lub dostarczyć dokumentację z większą ilością danych dotyczących długotrwałego stosowania), np. Izotek i Xarelto.

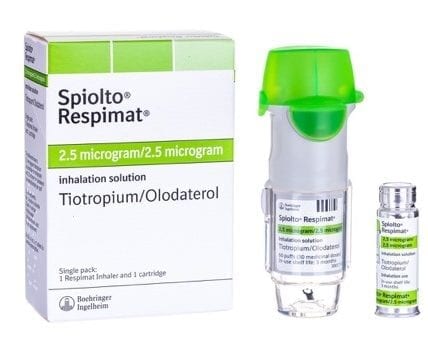
Czarnym trójkątem oznakowane są też leki zawierające nową substancję czynną dopuszczoną do obrotu po 1. stycznia 2011 roku, np. Spiolto Respimat.
Aktualny wykaz leków dodatkowo monitorowanych można znaleźć na stronie EMA. Wykaz jest co miesiąc weryfikowany przez PRAC (ang. Pharmacovigilance Risk Assessment Committee), czyli jeden z komitetów EMA, który jest odpowiedzialny za monitorowanie bezpieczeństwa leków. Lek podlega procedurze dodatkowego monitorowania przez okres około 5 lat.
Symbol odwróconego czarnego trójkąta nie powinien wzbudzać niepokoju. Powinien być dla pacjentów i pracowników ochrony zdrowia sygnałem, że należy zgłaszać działania niepożądane organom ds. rejestracji, bo jest to niezbędne to oceny bezpieczeństwa stosowania leku.[2][1]
 mgr farm. Marta Siarka
mgr farm. Marta SiarkaRedaktor w 3PG, współautorka podręczników dla farmaceutów. W 3PG zajmuje się głównie tematem opieki nad pacjentem onkologicznym, interesuje się też zagadnieniem stosowania opioidów i medycznej marihuany. Autorka artykułów i kursów dla farmaceutów.
Piśmiennictwo
- URPL: Leki podlegające dodatkowemu monitorowaniu pełny tekst⬏⬏
- European Medicines Agency: Co oznacza czarny trójkąt? pełny tekst.pdf⬏















