Poznaj leki Bronchipret®


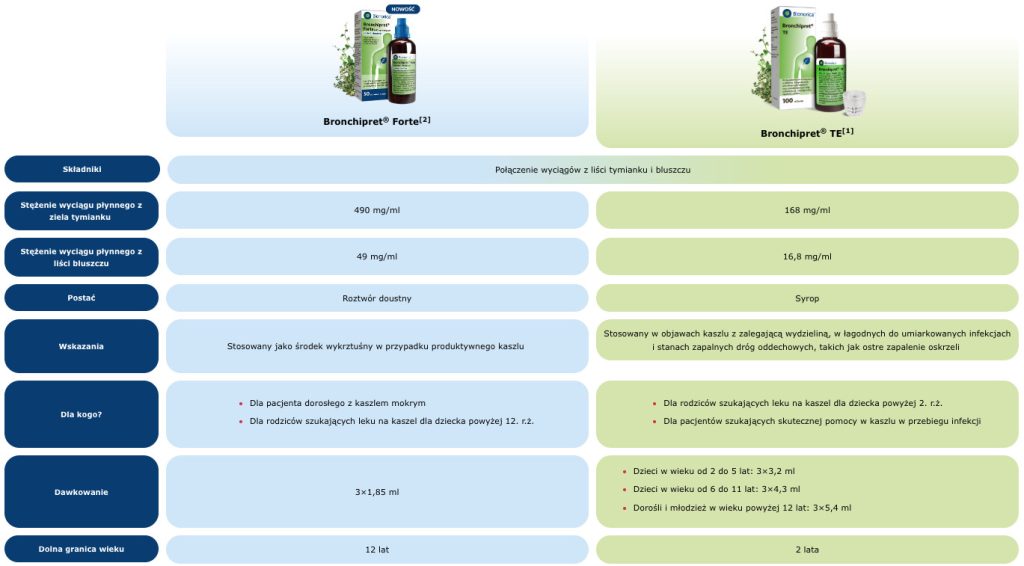
Bronchipret® Forte[2]

Bronchipret® TE[1]
Składniki
Połączenie wyciągów z liści tymianku i bluszczu
Stężenie wyciągu płynnego z ziela tymianku
490 mg/ml
168 mg/ml
Stężenie wyciągu płynnego z liści bluszczu
49 mg/ml
16,8 mg/ml
Postać
Roztwór doustny
Syrop
Wskazania
Stosowany jako środek wykrztuśny w przypadku produktywnego kaszlu
Stosowany w objawach kaszlu z zalegającą wydzieliną, w łagodnych do umiarkowanych infekcjach i stanach zapalnych dróg oddechowych, takich jak ostre zapalenie oskrzeli
Dla kogo?
- Dla pacjenta dorosłego z kaszlem mokrym
- Dla rodziców szukających leku na kaszel dla dziecka powyżej 12. r.ż.
- Dla rodziców szukających leku na kaszel dla dziecka powyżej 2. r.ż.
- Dla pacjentów szukających skutecznej pomocy w kaszlu w przebiegu infekcji
Dawkowanie
3×1,85 ml
- Dzieci w wieku od 2 do 5 lat: 3×3,2 ml
- Dzieci w wieku od 6 do 11 lat: 3×4,3 ml
- Dorośli i młodzież w wieku powyżej 12 lat: 3×5,4 ml
Dolna granica wieku
12 lat
2 lata
Nowy lek redukujący napady kaszlu o 50% Sprawdź co polecić pacjentowi
Przeczytaj artykuł i sprawdź, co pokazują badania
Co wiemy o skuteczności leków Bronchipret®?
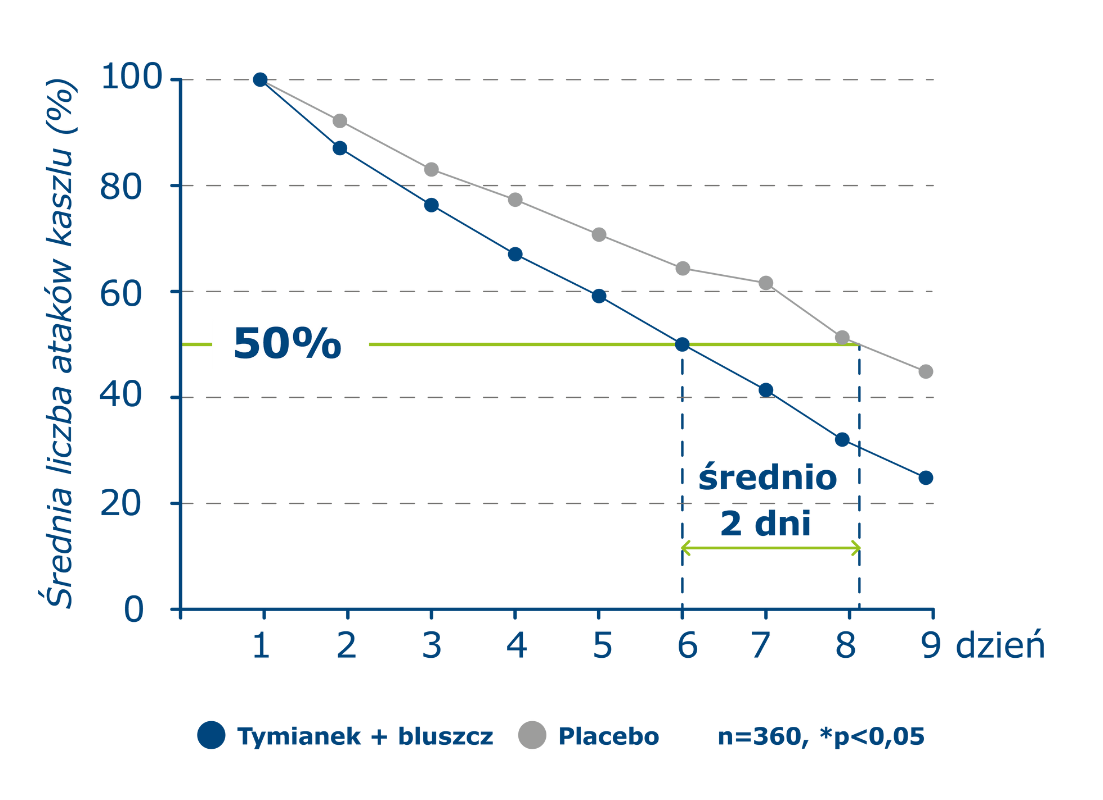

Badanie: randomizowane kontrolowane placebo, podwójnie zaślepione, wieloośrodkowe.[3]

Grupa badana: 361 pacjentów, w wieku od 18 do 87 lat, z ostrym zapaleniem oskrzeli i kaszlem produktywnym.[3]

Czas trwania leczenia: 10 dni.[3]

Leczenie: grupa badana (182 pacjentów) otrzymywała lek Bronchipret® TE wg dawkowania przedstawionego w ChPL, grupa kontrolna (179 pacjentów) otrzymywała placebo.[3]
Wnioski z badania

Zmniejszenie liczby napadów kaszlu – redukcja liczby napadów kaszlu o 50% osiągnięta o 2 dni szybciej niż w grupie placebo.[3]

Lepsza i szybsza poprawa w skali nasilenia objawów zapalenia oskrzeli (BSS) – (ang. Bronchitis Severity Score) poprawiał się znacznie szybciej w grupie leczonej lekiem Bronchipret®. Różnice były widoczne już podczas pierwszej kontroli.[3]

Leczenie było dobrze tolerowane – częstość działań niepożądanych była podobna do placebo, a ponadto nie zanotowano poważnych działań niepożądanych.[3]

Badanie: nieinterwencyjne, obserwacyjne badanie dotyczące leczenia ostrego zapalenia oskrzeli u dzieci i młodzieży lekiem Bronchipret® TE.[4]

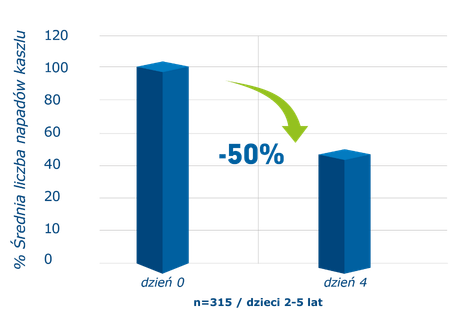
Grupa badana: 1234 dzieci i młodzieży w wieku od 2 do 17 lat z ostrym zapaleniem oskrzeli i produktywnym kaszlem. W tym grupa 315 dzieci w wieku 2-5 lat.[4]


Leczenie: pacjenci otrzymywali wiekowo dostosowane dawki syropu zawierającego ekstrakty z tymianku i bluszczu zgodnie ze wskazaniami ChPL.[4]
Wnioski z badania

Redukcja liczby napadów kaszlu – liczba napadów kaszlu w grupie dzieci w wieku 2-5 lat zmniejszyła sie średnio o 50% już 4. dnia terapii.[4]
Wysokie wskaźniki odpowiedzi na leczenie — 92–96 % pacjentów wykazało poprawę w zakresie ustępowania objawów.[4]

Dlaczego warto zarekomendować pacjentowi Bronchipret® TE i Bronchipret®Forte?


Mają skuteczność udowodnioną badaniami klinicznymi – nie są to kolejne wyroby medyczne czy suplementy diety, a leki.[1,2]




Odpowiednie nawet dla astmatyków i pacjentów z chorobą wrzodową – nie są przeciwwskazane w tych stanach, jak np. karbocysteina przy chorobie wrzodowej[5,6] czy kodeina u pacjentów z astmą oskrzelową.[8]

Nie zawierają cukru, laktozy ani glutenu – są bezpieczne dla szkliwa zębów, diabetyków oraz osób z nietolerancją laktozy i glutenu.[1,2]


Mają długi okres trwałości po otwarciu – mogą być stosowane do 6 miesięcy od pierwszego użycia, co ułatwia ich przechowywanie i stosowanie w domu.[1,2]
Komu w szczególności warto polecić leki Bronchipret®?

Karol, 30 lat
Dorosły z kaszlem mokrym
Interwencja
Zarekomendowano lek Bronchipret® Forte, którego skuteczność została udowodniona w badaniach klinicznych.
Uzasadnienie interwencji

Julian, 2 lata
2-latek z kaszlem infekcyjnym
Interwencja
Zalecono syrop Bronchipret® TE odpowiedni dla pacjentów już od 2. r.ż.
Uzasadnienie interwencji

Marian, 75 lat
Starszy pacjent z kaszlem mokrym
Interwencja
Uzasadnienie interwencji
Jest to roślinny produkt leczniczy, który nie wykazuje interakcji z innymi lekami, ani nie powoduje częstych ani bardzo częstych działań niepożądanych. Lek w postaci roztworu doustnego jest formą łatwą do połknięcia, co jest istotne dla pacjentów starszych, którzy moją problem z przyjmowaniem leków.[9]

Konkurs zakończony. Dziękujemy za zainteresowanie.
Nazwa produktu leczniczego: Bronchipret TE.
Skład:
100 ml (co odpowiada 112 g) syropu zawiera:
16,8 g płynnego wyciągu z Thymus vulgaris L. i(lub) Thymus zygis L., herba (tymianek) (1:2-2,5). Rozpuszczalnik ekstrakcyjny: roztwór amoniaku 10% (m/m) / glicerol (85%) (m/m) / etanol 90% (V/V) / woda oczyszczona (1/20/70/109).
1,68 g płynnego wyciągu z Hedera helix L., folium (liść bluszczu) (1:1). Rozpuszczalnik ekstrakcyjny: etanol 70% (V/V).
Ten produkt leczniczy zawiera 7% [V/V] alkoholu.
Substancje pomocnicze o znanym działaniu:
1 ml syropu zawiera 423 mg maltitolu ciekłego, 28,76 mg sorbitolu (sorbitol zawarty w maltitolu ciekłym).
Postać farmaceutyczna: Syrop
Wskazania terapeutyczne do stosowania: Produkt leczniczy roślinny stosowany w objawach kaszlu z zalegającą wydzieliną, w łagodnych do umiarkowanych infekcjach i stanach zapalnych dróg oddechowych, takich jak ostre zapalenie oskrzeli.
Dawkowanie i sposób podawania: Dzieci w wieku od 2 do 5 lat – 3,2 ml 3 razy na dobę.
Dzieci w wieku od 6 do 11 lat – 4,3 ml 3 razy na dobę. Dorośli i młodzież w wieku powyżej 12 lat – 5,4 ml 3 razy na dobę. Podanie doustne. Syrop należy połknąć bez rozcieńczania. Lek można popić niewielką ilością płynu (najlepiej wody). Butelkę wstrząsnąć przed użyciem. W przypadku dolegliwości utrzymujących się ponad 10 dni lub w przypadku pojawienia się trudności w oddychaniu, gorączki, bądź ropnej lub krwistej wydzieliny, wymagana jest pilna konsultacja lekarska.
Przeciwwskazania: Nadwrażliwość na substancje czynne oraz na inne rośliny z rodziny jasnotowatych (Lamiaceae) oraz araliowatych (Araliaceae), brzozę, bylicę pospolitą, seler, lub na którąkolwiek substancję pomocniczą.
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania:
W przypadku dolegliwości utrzymujących się ponad 10 dni lub pojawienia się trudności w oddychaniu, gorączki bądź ropnej lub krwistej wydzieliny, lekarz powinien skonsultować stan pacjenta i zadecydować o dalszym leczeniu. Należy zachować ostrożność stosując lek u pacjenta z zapaleniem bądź owrzodzeniem błony śluzowej żołądka. Produkt leczniczy zawiera 7% obj. alkoholu, oznacza to, że 5,4 ml zawiera do 300 mg alkoholu (etanolu), co jest równoważne 8 ml piwa lub 3 ml wina. Podanie dawki 3,2 ml tego produktu leczniczego dwuletniemu dziecku o masie ciała 11,5 kg spowoduje narażenie na 15,65 mg/kg etanolu, co może spowodować wzrost stężenia alkoholu we krwi (BAC) o około 2,61 mg/100 ml. Dla porównania, u osoby dorosłej po wypiciu kieliszka wina lub 500 ml piwa, BAC prawdopodobnie wyniesie około 50 mg/100 ml. Jednoczesne podawanie z produktami leczniczymi zawierającymi m.in. glikol propylenowy lub etanol może prowadzić do kumulacji etanolu i wywoływać działania niepożądane, szczególnie u małych dzieci z niską lub niedojrzałą zdolnością metaboliczną. Pacjenci z rzadkimi dziedzicznymi zaburzeniami związanymi z nietolerancją fruktozy nie powinni przyjmować produktu leczniczego Bronchipret TE. Produkt leczniczy nie powinien być podawany dzieciom w wieku poniżej 2 lat. W przypadku dłużej utrzymującego się lub nawracającego kaszlu u dzieci w wieku pomiędzy 2 a 4 rokiem życia, lekarz powinien ocenić objawy, gdyż mogą one być oznaką ciężkiego przebiegu choroby.
Działania niepożądane: Zaburzenia żołądka i jelit: zaburzenia żołądkowo-jelitowe, np. skurcze, nudności, wymioty, biegunka (niezbyt często). Zaburzenia układu immunologicznego: obserwowano reakcje nadwrażliwości przebiegające z wysypką (rzadko). Mogą również wystąpić takie reakcje nadwrażliwości jak: duszność wysiłkowa, pokrzywka i obrzęk twarzy, ust i (lub) okolicy gardła (częstość nieznana). W przypadku pojawienia się pierwszych objawów nadwrażliwości lub reakcji alergicznych, należy natychmiast przerwać stosowanie produktu leczniczego Bronchipret TE.
Podmiot odpowiedzialny: Bionorica SE, 92308 Neumarkt, Niemcy. Informacji o leku udziela: Bionorica Polska Sp. z o.o., ul. Hrubieszowska 6B, 01-209 Warszawa.
Numer pozwolenia na dopuszczenie do obrotu: Pozwolenie nr 23507 wydane przez Prezesa URPL,WMiPB.
OTC – Produkt leczniczy wydawany bez recepty.
Nazwa produktu leczniczego: Bronchipret Forte, roztwór doustny, (490 mg + 49 mg)/ml Skład: 1 ml (co odpowiada 1,09 g) roztworu zawiera: 490 mg wyciągu płynnego z Thymus vulgaris L. i(lub) Thymus zygis L., herba lub ich mieszanina (ziele tymianku) 1:2-2,5). Rozpuszczalnik ekstrakcyjny: roztwór amoniaku 10% m/m / glicerol 85% m/m / etanol 90% v/v / woda oczyszczona (1/20/70/109). 49 mg wyciągu płynnego z Hedera helix L., folium (liść bluszczu) (1:1). Rozpuszczalnik ekstrakcyjny: etanol 70% v/v. Substancje pomocnicze o znanym działaniu: maltitol ciekły: 272 mg, sorbitol (zawarty w maltitolu, ciekłym): 18,5 mg, etanol: całkowita zawartość alkoholu maksymalnie 15% m/m, co odpowiada maksymalnie 21% v/v. Postać farmaceutyczna: Roztwór doustny. Wskazanie do stosowania: Produkt leczniczy roślinny stosowany jako środek wykrztuśny w przypadku produktywnego kaszlu dla dorosłych i młodzieży w wieku od 12 lat. Dawkowanie i sposób podawania: Dorośli i młodzież w wieku od 12 lat: 1,85 ml trzy razy na dobę. Maksymalna dawka wynosi 5,55 ml na dobę. Produkt leczniczy Bronchipret Forte należy połknąć bez rozcieńczenia. Po zażyciu produkt leczniczy należy popić niewielką ilością płynu (najlepiej wody). Przeciwwskazania: Nadwrażliwość na substancje czynne, na inne gatunki roślin z rodziny Lamiaceae lub na którąkolwiek substancję pomocniczą. Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania: Pacjent powinien skonsultować się z lekarzem lub farmaceutą jeżeli objawy utrzymują się ponad 7 dni lub ulegną zaostrzeniu podczas stosowania produktu leczniczego. W razie wystąpienia duszności, gorączki lub ropnej plwociny pacjent powinien skonsultować się z lekarzem lub farmaceutą. Należy zachować ostrożność u pacjentów z zapaleniem błony śluzowej żołądka lub chorobą wrzodową żołądka i dwunastnicy. Pacjenci z zapaleniem lub owrzodzeniem błony śluzowej żołądka powinni przed zastosowaniem produktu leczniczego Bronchipret Forte skonsultować się z lekarzem. Produkt leczniczy zawiera maltitol, ciekły (zawiera sorbitol (E420)). Ten produkt leczniczy zawiera 34,20 mg sorbitolu w każdym 1,85 ml (pojedyncza dawka), co odpowiada 18,5 mg/ml. Produkt leczniczy nie powinien być stosowany u pacjentów z rzadko występującą dziedziczną nietolerancją fruktozy. Ten produkt leczniczy zawiera ok. 310 mg alkoholu (etanol) w każdym 1,85 ml (pojedyncza dawka), co odpowiada 168 mg/ml (15% m/m). Ilość alkoholu zawarta w 1,85 ml tego produktu leczniczego jest równoważna mniej niż 8 ml piwa lub 4 ml wina. Mała ilość alkoholu zawarta w tym produkcie nie będzie powodowała zauważalnych skutków. Działania niepożądane: Zaburzenia układu odpornościowego Rzadko (≥ 1/10 000 do < 1/1000): nadwrażliwość i (lub) reakcje alergiczne z wysypką. Częstość nieznana (nie może być określona na podstawie dostępnych danych): nadwrażliwość i (lub) reakcje alergiczne takie jak duszność, pokrzywka, obrzęk twarzy, jamy ustnej i (lub) krtani, reakcja anafilaktyczna. Zaburzenia żołądka i jelit Niezbyt często (≥ 1/1 000 do < 1/100): zaburzenia żołądka i jelit, takie jak skurcze, nudności, wymioty, biegunka. W przypadku wystąpienia pierwszych objawów nadwrażliwości i (lub) reakcji alergicznej, nie należy przyjmować produktu leczniczego Bronchipret Forte ponownie. Podmiot odpowiedzialny: Bionorica SE, 92308 Neumarkt, Niemcy. Informacji o leku udziela: Bionorica Polska Sp. z o.o., ul. Hrubieszowska 6B, 01-209 Warszawa Numer pozwolenia na dopuszczenie do obrotu: Pozwolenie nr 28929 wydane przez Prezesa URPL,WMiPB. OTC – Produkt leczniczy wydawany bez recepty
Piśmiennictwo:
- Bionorica. (b.d.). ChPL Bronchipret TE
- Bionorica. (b.d.). ChPL Bronchipret Forte
- Kemmerich, B., Eberhardt, R., & Stammer, H. (2006). Efficacy and tolerability of a fluid extract combination of thyme herb and ivy leaves and matched placebo in adults suffering from acute bronchitis with productive cough. A prospective, double-blind, placebo-controlled clinical trial. Arzneimittel-Forschung, 56(9), 652–660. https://doi.org/10.1055/s-0031-1296767
- Marzian O. (2007). Behandlung der akuten Bronchitis bei Kindern und Jugendlichen. Anwendungsbeobachtung bestätigt Nutzen und Unbedenklichkeit einer Flüssigextrakt-Kombination aus Thymiankraut und Efeublättern [Treatment of acute bronchitis in children and adolescents. Non-interventional postmarketing surveillance study confirms the benefit and safety of a syrup made of extracts from thyme and ivy leaves]. MMW Fortschritte der Medizin, 149(27-28 Suppl), 69–74.
- Adamed. (b.d.) ChPL Mucopect Kids
- Polpharma. (2017). ChPL Flegamax
- Rakshana, S., Chamarthi, V. R., Kothimbakkam, S. S. K., Kalaivanan, D., Krishnamoorthy, S., Saleem, S., & AKR, S. P. (2024). Therapy or damage usage of paracetamol syrup and its adverse dental effects in children of age 0–6 years. International Journal of Applied Dental Sciences, 10(2), 172–174. https://doi.org/10.22271/oral.2024.v10.i2c.1938
- Unia ChPL Thiocodin
- Belissa, E., Vallet, T., Laribe Caget, S., Chevallier, A., Chedhomme, F.-X., Abdallah, F., Bachalat, N., Belbachir, S.-A., Boulaich, I., Bloch, V., … Boudy, V. (2019). Acceptability of oral liquid pharmaceutical products in older adults: Palatability and swallowability issues. BMC Geriatrics, 19, Article 344. https://doi.org/10.1186/s12877-019-1337-2

Materiał przygotowany
we współpracy z firmą BIONORICA.
2026/01/ST/BRO